拠点メンバーの登田特任教授・湯川格史助教のグループとフランシス・クリック研究所の2つのグループ(Thomas Surrey and Martin R. Singleton)間の共同研究の成果がJournal of Cell Scienceの電子版に掲載されました。
ヒトまで広く保存されている分裂酵母微小管結合タンパク質Dis1/TOGとMal3/EB1が、今まで知られていなかった新規の構造形態で直接結合することによって、染色体分離の正確さを制御していることが明らかになりました。
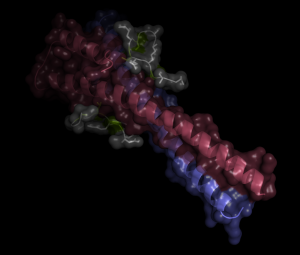
下に示したイメージは、X線結晶解析をもとに作られたDis1由来の21残基ペプチド(837AGSMLQKPTQFSRP849)とMal3/EB1が形成する複合体構造です。Dis1は既知のモチーフ(SXIP)ではなく、今回発見された新規のアミノ酸配列(L841, P844 and F847)がそれぞれMal3/EB1に存在する疎水性アミノ酸群からなる窪み部と直接相互作用することによって結合します。
論文情報
An unconventional interaction between Dis1/TOG and Mal3/EB1 promotes the fidelity of chromosome segregation
Yuzy Matsuo, Sebastian P. Maurer, Masashi Yukawa, Silva Zakian, Martin R. Singleton, Thomas Surrey and Takashi Toda
【Abstract】